De Dois Exemplos De Cada Transformações De Estado Dos Materiais: A gente mergulha fundo no mundo fascinante das mudanças de estado da matéria, explorando como sólidos viram líquidos, líquidos viram gases, e até mesmo sólidos pulam direto pra gasoso, numa mágica da natureza que a gente vai desvendar aqui. Prepara o cafezinho e vem com a gente nessa jornada científica, que vai te deixar de queixo caído!
Vamos explorar os três estados clássicos – sólido, líquido e gasoso – entendendo a dança das moléculas e a energia que faz tudo acontecer. A partir daí, a gente vai analisar transformações específicas, com exemplos do dia a dia e da indústria, mostrando como essas mudanças impactam nosso mundo. Prepare-se para uma imersão completa no universo microscópico que governa tudo ao nosso redor!
Transformações de Estado da Matéria: Um Olhar Descolado: De Dois Exemplos De Cada Transformações De Estado Dos Materiais
A matéria, essa galera toda que compõe o nosso universo, não fica parada não! Ela adora mudar de forma, de estado, sabe? A gente vai mergulhar nesse mundo fascinante das transformações de estado, de um jeito casual e maneiro, explorando os três estados principais: sólido, líquido e gasoso, e as diversas “fases” que eles podem passar. Prepare-se para uma viagem molecular!
Os Três Estados Físicos da Matéria
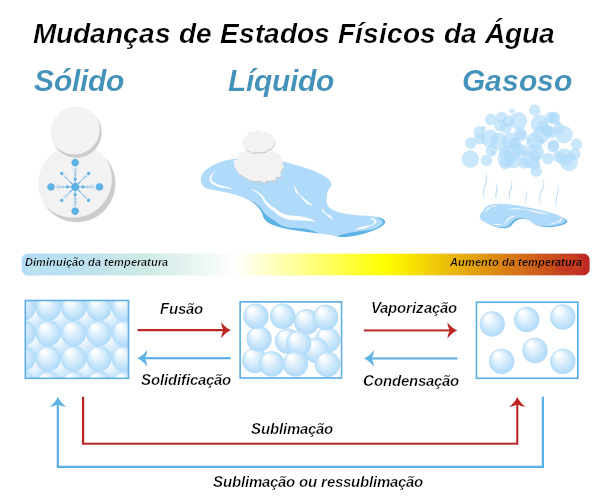
Tudo começa com os três estados clássicos: sólido, líquido e gasoso. No estado sólido, as partículas (átomos, moléculas, íons) estão bem juntinhas, organizadas em uma estrutura rígida, com pouca energia cinética (movimento). Já no líquido, elas têm mais liberdade, se movimentam mais, a organização é menos rígida, e a energia cinética é maior. E no estado gasoso? É a festa! As partículas estão super espalhadas, com alta energia cinética e quase nenhuma organização.
Transições de Fase Entre os Estados
A matéria adora uma transformação! As mudanças de estado são chamadas de transições de fase, e elas acontecem quando a energia (geralmente na forma de calor) é adicionada ou removida. Vamos dar uma olhada nas principais transições:
| Estado Inicial | Estado Final | Nome da Transição | Descrição do Processo |
|---|---|---|---|
| Sólido | Líquido | Fusão | Aquecimento aumenta a energia cinética, quebrando as ligações e tornando o sólido líquido. |
| Líquido | Sólido | Solidificação | Resfriamento diminui a energia cinética, permitindo que as partículas se organizem em uma estrutura sólida. |
| Líquido | Gasoso | Vaporização (Ebulição/Evaporação) | Aquecimento fornece energia para as partículas superarem as forças intermoleculares e se tornarem gasosas. |
| Gasoso | Líquido | Liquefação (Condensação) | Resfriamento reduz a energia cinética, fazendo com que as partículas se aproximem e formem um líquido. |
| Sólido | Gasoso | Sublimação | As partículas passam diretamente do estado sólido para o gasoso sem passar pelo estado líquido. |
| Gasoso | Sólido | Deposição | As partículas passam diretamente do estado gasoso para o sólido sem passar pelo estado líquido. |
Exemplos de Transformações Sólido-Líquido e Vice-versa, De Dois Exemplos De Cada Transformações De Estado Dos Materiais

Vamos ver alguns exemplos práticos dessas transformações!
Fusão (Sólido para Líquido)
| Material | Descrição da Fusão |
|---|---|
| Gelo | Ao ser aquecido, o gelo absorve energia, suas moléculas vibram mais e rompem as ligações de hidrogênio, transformando-se em água líquida. |
| Chumbo | O chumbo, um metal, funde-se a uma temperatura relativamente baixa (327°C), tornando-se um líquido brilhante e maleável. |
Solidificação (Líquido para Sólido)
| Material | Descrição da Solidificação |
|---|---|
| Água | Ao ser resfriada abaixo de 0°C, a água líquida libera energia, suas moléculas diminuem a velocidade e se organizam em uma estrutura cristalina, formando gelo. |
| Ferro | O ferro derretido, em altas temperaturas, solidifica-se ao ser resfriado, formando uma estrutura sólida e rígida. Este processo é crucial na metalurgia. |
Em ambos os processos, a energia é chave: na fusão, energia é absorvida; na solidificação, energia é liberada.
Exemplos de Transformações Líquido-Gasoso e Vice-versa

Agora, vamos ver as transformações entre líquido e gasoso. Aqui temos a ebulição (vaporização em todo o líquido) e a evaporação (vaporização na superfície).
Vaporização (Líquido para Gasoso)
- Ebulição da água: Ao atingir 100°C (ao nível do mar), a água entra em ebulição, transformando-se rapidamente em vapor d’água. Bolhas de vapor se formam em todo o líquido.
- Evaporação da água em um lago: Em um dia quente e ensolarado, a água de um lago evapora gradualmente. As moléculas de água na superfície ganham energia suficiente para escapar para a atmosfera.
Liquefação (Gasoso para Líquido)
- Condensação do vapor d’água: O vapor d’água na atmosfera se condensa em gotículas de água quando encontra uma superfície fria, como um copo gelado.
- Liquefação do gás natural: O gás natural é resfriado e comprimido para ser transformado em líquido, facilitando o transporte e armazenamento.
Pressão e temperatura são fundamentais: altas temperaturas favorecem a vaporização, enquanto baixas temperaturas e alta pressão favorecem a liquefação.
Exemplos de Sublimação e Deposição
Sublimação e deposição são transições de fase um pouco mais “exóticas”, mas igualmente interessantes!
Sublimação (Sólido para Gasoso)
- Gelo seco (dióxido de carbono sólido): O gelo seco sublima diretamente para o dióxido de carbono gasoso à temperatura ambiente, criando um efeito de “fumaça”.
- Naftalina: As pastilhas de naftalina, usadas para repelir insetos, sublimam lentamente, liberando vapores que se espalham pelo ar.
Deposição (Gasoso para Sólido)
- Formação de geada: O vapor d’água na atmosfera pode depositar-se diretamente como cristais de gelo em superfícies frias.
- Formação de neve: O vapor d’água na atmosfera pode se transformar diretamente em cristais de gelo, formando flocos de neve.
Sublimação e deposição diferem das outras transições por envolverem a passagem direta entre os estados sólido e gasoso, sem passar pelo estado líquido.
Fatores que Influenciam as Transformações de Estado
Vários fatores influenciam as temperaturas de transição de fase.
| Fator | Efeito na Transição | Exemplo |
|---|---|---|
| Temperatura | Aumenta a energia cinética das partículas, favorecendo transições para estados menos ordenados (sólido para líquido, líquido para gasoso). | O gelo derrete a 0°C, a água ferve a 100°C (ao nível do mar). |
| Pressão | A alta pressão favorece estados mais densos (líquido e sólido), enquanto baixa pressão favorece estados menos densos (gasoso). | A água ferve a uma temperatura mais baixa em altitudes elevadas (menor pressão). |
| Forças intermoleculares | Forças intermoleculares fortes requerem mais energia para que ocorra a transição de fase. | A água tem um ponto de ebulição mais alto que o éter devido às fortes ligações de hidrogênio. |
Aplicações das Transformações de Estado
As transformações de estado são super importantes em várias aplicações!
Aplicações da Fusão
- Fundição de metais: A fusão de metais é essencial na produção de peças metálicas, como carros, máquinas e utensílios.
- Reciclagem de plásticos: O plástico é fundido para ser transformado em novos produtos.
Aplicações da Vaporização
- Refrigeração: A vaporização de refrigerantes em sistemas de refrigeração retira calor do ambiente.
- Destilação: A vaporização e condensação são usadas para separar componentes de misturas.

